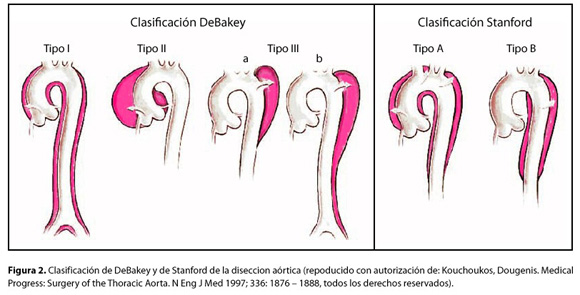
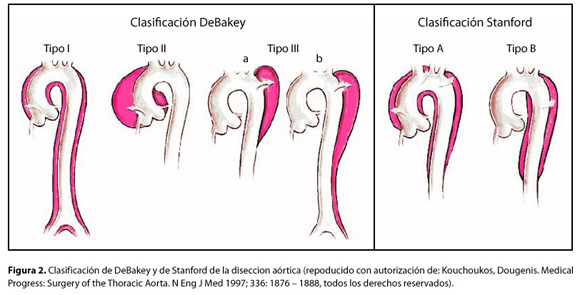
Cada año, la disección aórtica afecta a uno de cada 20.000 personas,1 2 resultando en 3.000 muertes en los Estados Unidos. Los hombres son afectados dos veces más que las mujeres, y la mayoría de las personas afectadas son mayores de 65 años1 2 Dos tercios de las disecciones involucran a la aorta ascendente (tipo A), y muchos de estos pacientes mueren antes de llegar a hospital.1 Los sobrevivientes, que suelen tratarse con cirugía inmediata (abierta o endovascular) a menos que esté contraindicado, tiene una mortalidad de 30 días de 20 a 50%.1 2 3
Las disecciones limitadas a la aorta descendente (tipo B) por lo general se resuelven sin reparación a menos que se presenten complicaciones, 2 4 y con este enfoque tienen una mortalidad a los 30 días de alrededor de 12%.1 3
Durante casi medio siglo, el manejo médico inicial recomendado de la disección aórtica aguda de ambos tipos ha sido "agresivo" con reducción de la presión arterial sistólica por debajo de 100 o 120 mm Hg y de la frecuencia cardiaca por debajo de 60 latidos por minuto, con el uso en primera línea de β bloqueantes intravenosos.4 5
"Las caídas excesivas de la tensión arterial pueden precipitar isquemia renal, cerebral o coronaria que deben ser evitadas"
Estas recomendaciones para la disección aórtica son notables a la luz de la creciente conciencia en otras áreas de la medicina de los riesgos del tratamiento intensivo en general y en relación con la presión arterial en particular.6 7 Luego de una serie de informes de eventos adversos después un descenso rápido de la presión arterial en hipertensos en emergencias,7 los informes del sexto y séptimo Comité Nacional Conjunto de Prevención, Detección, Evaluación y Tratamiento de la Hipertensión Arterial (JNC) recomienda bajar la presión arterial media en no más del 25% en cuestión de minutos a una hora, después hasta 160/100 mm Hg en las próximas dos a seis horas, y señalan que "las caídas excesivas de la tensión arterial pueden precipitar isquemia renal, cerebral o coronaria que deben ser evitadas"8 Sin embargo, se hizo una excepción para los "pacientes con disección aórtica que deben tener su presión arterial sistólica a <100 mm Hg si se tolera.
"El uso en primera línea de bloqueadores β también difiere de las recomendaciones para los pacientes sin disección aórtica que tienen hipertensión o que se someten a cirugía, para quien esta práctica no se recomienda debido a la evidencia de un aumento de la morbilidad cardiovascular y mortalidad.9 10 11
El control a largo plazo de la presión arterial sistólica por debajo de 120 mm Hg después de la disección aórtica (con o sin cirugía) también está ampliamente recomendado,5 suele requerir cinco o más fármacos,12 y contrasta con las recomendaciones para los pacientes mayores de 60 años sin disección aórtica, para quienes el objetivo de presión arterial sistólica recientemente se ha elevado a 150 mm Hg.9
¿Cuál es la evidencia de la incertidumbre?
Se buscaron evidencias en Medline (aneurisma, disección), en la Biblioteca Cochrane, y en las listas de referencias de artículos pertinentes. Ni nosotros ni una reciente revisión Cochrane encontró ensayos aleatorios sobre el tratamiento médico de disección aórtica.13
El primer uso reportado de tratamiento médico intensivo fue el trabajo de Trigo y Palmer en 1965.14 Seis de sus pacientes tratados médicamente sobrevivieron, en contra de su experiencia previa de ningún superviviente entre los seis pacientes tratados con cirugía. Su régimen médico fue dirigido a limitar la extensión de la disección mediante la reducción de la fuerza del impulso cardíaco e implicó la reducción de la presión arterial sistólica hasta aproximadamente 100 mm de Hg mediante el uso de fármacos con un efecto inotrópico negativo.
Los autores fueron influenciados por un informe sobre disección aórtica que ocurrió en nueve de 44 pacientes con hipertensión grave tratados con hexametonio, un fármaco antihipertensivo con un efecto inotrópico positivo, y por los informes de que la disección aórtica puede ser prevenida en los pavos de granja susceptibles por el tratamiento crónico con fármacos inotrópicos negativos como reserpina y propranolol, aunque esto ocurrió incluso a dosis que no afectan la presión arterial o la frecuencia cardíaca.15
Más resultados aceptables en pacientes con disección manejados con un tratamiento médico intensivo se registraron posteriormente en series de unas pocas docenas de pacientes por los autores originales y por otros.14 15 Sin embargo, el tipo A y B de disecciones no solían distinguirse antes de 1970, por lo que las comparaciones entre cirugía y tratamiento médico en estas primeras series son problemáticas.
Más apoyo para tratamiento médico intensivo provino de los estudios de laboratorio en los que se muestran "desgarros de la íntima" hechos en aortas sintéticas que se extienden cuando la intensidad del flujo pulsátil (pero no laminar) excede un calor umbral.15 Estudios posteriores en perros demostraron que la extensión de un desgarro de la íntima introducido fue minimizado por las drogas que reducen la presión arterial y el inotropismo.16
Estos estudios en laboratorio sugieren un efecto beneficioso del tratamiento intensivo sobre la disección de la aorta, pero no pudieron evaluar su efecto global sobre el paciente. Ya en 1967, los médicos informaban que "las complicaciones debidas a la terapia hipotensora fueron significativas".17
Si el tratamiento médico intensivo salvó más vidas mediante la prevención de la extensión de la disección de las que se perdieron por las consecuencias adversas de la hipotensión es algo que rara vez fue considerado. En la única comparación directa que identificamos, ocho pacientes que no recibieron tratamiento para la disección tipo B y nueve pacientes tratados con el tratamiento médico intensivo tenían tasas de supervivencia equivalentes.18 Muchos pacientes con disección presentaban hipertensión grave (tres de seis pacientes originales de Trigo tenían presiones arteriales por encima de 200/140 mm Hg), por lo que, aunque la reducción de la presión arterial es a menudo claramente necesaria, se ha dado poca consideración a los regímenes más moderados.
Desde los primeros informes, la investigación de un tratamiento médico intensivo se ha limitado a un puñado de series de casos. En estas series, en los pacientes que cumplieron con éxito un objetivo específico de tratamiento intensivo durante o después de la admisión hospitalaria inicial de la disección aórtica aguda se encontró que tenían un menor número de resultados adversos en los próximos años. Por ejemplo, un registro internacional informó asociaciones entre los medicamentos prescritos al alta hospitalaria y mejoras en la supervivencia a largo plazo, aunque la droga aparentemente beneficiosa difería según la localización de la disección (β bloqueantes para la disección tipo A y bloqueadores de los canales de calcio para la disección tipo B).19
Las preocupaciones con respecto a estos estudios incluyen muestras pequeñas (20-54 resultados adversos por estudio), la posibilidad de la selección post hoc de los predictores y medidas de resultado, los datos que faltan (especialmente en el registro), y, sobre todo, la posibilidad de que los resultados fueron peores debido a las razones por las que los pacientes no pudieron alcanzar las metas de tratamiento intensivo, más que a la falta de tratamiento en sí, como la terapia intensiva parece haber sido la intención de todos los pacientes.
Dado el florecimiento de pruebas de alta calidad en medicina cardiovascular en las últimas décadas, ¿cómo un tratamiento médico intensivo para la disección aórtica podría escapar al escrutinio de un ensayo aleatorio? Trigo y sus colegas declararon en 1969 que: "Hemos sido reacios a llevar a cabo una prueba de este tipo en el paciente humano. Creemos que la evidencia del modelo experimental en pavos es abrumadoramente convincente en este sentido".14
La experiencia moderna de las muchas reversiones de doctrinas aceptadas por evidencia posterior que hace que este tipo de convicción6 hoy hace a este tipo de declaraciones menos defendibles. Afirmaciones como: "Generalmente, cuando se reduce apropiadamente la presión arterial, el dolor del paciente se alivia dramáticamente"20 o "un resurgimiento repentino de impulso cardiaco y de la presión arterial después de que han sido disminuidas inicialmente puede ser desastroso”15 probablemente han desanimado la investigación y fomentaron una adhesión más dogmática al tratamiento intensivo.
La recomendación de los sociedades de cardiología para usar un tratamiento médico intensivo para la disección tiene clase I nivel C-la más fuerte de las recomendaciones basadas en la más débil de evidencia-.4
¿Es un tratamiento intensivo para la disección aórtica de un "paraguas", un tratamiento con un beneficio tan obvio que un estudio aleatorizado resulta innecesario?
Para que este sea el caso, el aparente beneficio del tratamiento debe tener primacía sobre el efecto combinado de los confundidores plausibles.21 Creemos que esta condición no se ha cumplido para el tratamiento médico intensivo de la disección aórtica. Ni el tamaño, ni siquiera la dirección del efecto de la hipotensión inducida puede estimarse a partir de los datos disponibles. En cuanto a la utilización preferente de los bloqueadores β, la reciente revisión Cochrane no encontró "fuerte fuente de evidencia de que un tipo de medicamento sea superior a otro".13
Las investigaciones en curso, ¿aportaran nuevas evidencias?
Se realizaron búsquedas de ensayos aleatorios en curso en ClinicalTrials.gov, registro maestro de la Organización Mundial de la Salud, y en una reciente revisión Cochrane13 y no encontramos ninguna. Los estudios observacionales no aportan pruebas suficientes, ya que son confundidos porque los pacientes no logran alcanzar las metas de tratamiento intensivo, como se señaló anteriormente.
¿Qué debemos hacer a la luz de la incertidumbre?
Ha llegado la hora de un ensayo aleatorizado de un tratamiento médico intensivo en pacientes con disección aórtica aguda. Mientras tanto, les sugerimos a los médicos que continúan utilizando un tratamiento intensivo que deben considerar moderarlo cuando surgen complicaciones como oliguria. Otros, que no estamos convencidos de sus beneficios y comparten nuestra preocupación sobre sus riesgos, podrían optar por utilizar un tratamiento menos intensivo como el descrito anteriormente de la Comisión Conjunta sobre otras emergencias hipertensivas, con una presión arterial que se baja sólo cuando sea necesario para controlar el dolor y sin tratar de frenar el ritmo sinusal.
Recomendación para futuras investigaciones
Este estudio podría incorporar un diseño factorial con una segunda asignación al azar para evaluar la reparación endovascular versus ninguna reparación de la disección de tipo B no complicada o versus cirugía abierta para la disección tipo A. |