Enfermedad pulmonar obstructiva crónica
Las comorbilidades y la edad avanzada modifican la presentación, las características de las exacerbaciones y el tratamiento clásicos de la enfermedad pulmonar obstructiva crónica.Autor: Dres. Raffaele Antonelli Incalzi, Simone Scarlata, Giorgio Pennazza c, Marco Santonico, Claudio Pedone. European Journal of Internal Medicine 25 (2014) 320–328
La EPOC adquiere características particulares en las personas ancianas lo que hace necesario un abordaje integral que tome en cuenta el proceso de envejecimiento, las comorbilidades y la particular respuesta al tratamiento en este grupo etario.
¿Es la EPOC una patología crónica relacionada con la edad?
La EPOC es una enfermedad típica del envejecimiento cuya prevalencia aumenta drásticamente con la edad. En EE. UU. oscila entre el 6,6 % en el grupo de 45-54 años hasta un 12 % a partir de los 64 años. Los datos relativos de los países europeos solo se refieren a los adultos de la población general y no a la población geriátrica.
La EPOC es responsable de la mayoría de la oxigenoterapia prolongada, sobre todo en los >70 años, comparados con la población general. Estos hallazgos reflejan los efectos acumulativos del tabaquismo y la polución ambiental.
Por otra parte, el acortamiento de los telómeros, un signo distintivo del proceso de envejecimiento, también aparece en los pacientes con EPOC, así que la edad junto con la EPOC, lo promueven su ocurrencia. Se destaca que la disfunción de la telomerasa y el acortamiento acelerado de los telómeros son también comunes en las células endoteliales que participan en el proceso aterosclerótico, condiciones prototípicas relacionadas con la edad, así como con las enfermedades inmunológicas como la artritis reumatoidea, las cuales están estrictamente relacionadas con la edad. Parece haber una base biológica clara que subyace en la evidencia epidemiológica, aunque el vínculo entre la EPOC y la telomerasa defectuosa debe ser distinguido de los efectos de las infecciones previas, como la infección por Citomegalovirus.
Hay otras similitudes entre el envejecimiento del pulmón y el pulmón de la EPOC que son dignas de mención:
En el envejecimiento normal, la capacidad vital declina anualmente 10-20 ml, mientras que en los pacientes con EPOC la declinación es de unos 30 ml; el volumen residual aumenta tanto en el envejecimiento normal como en el pulmón de la EPOC. Por otra parte, en las personas mayores hay una pérdida de la elasticidad, la depuración mucociliar, la inmunidad de la mucosa y la reserva vascular, más acentuada en la EPOC. A pesar de la estrecha relación con la edad, la prevalencia de la EPOC en los ancianos no se conoce por completo. En efecto, tanto los cambios relacionados con la edad que aparecen en la presentación clínica de la EPOC como el enmascaramiento derivado de las comorbilidades, sumado a los problemas para ejecutar la espirometría contribuyen a obstaculizar el diagnóstico de la enfermedad en la población de edad avanzada.

¿Por qué es difícil el diagnóstico de la EPOC en la población de edad avanzada?
Aun las exacerbaciones graves de la EPOC pueden ser reconocidas tardíamente debido a una presentación atípica. En efecto, a diferencia de la triada clásica de disnea, tos y fiebre, la EPOC también puede presentarse con debilidad muscular, vértigo, confusión y edema de las piernas, cuadros que reflejan una hipoxemia grave y que son característicos de las presentaciones atípicas, en ocasiones también el delirio puede ser la principal manifestación.
El aumento del umbral de disnea y la discapacidad física relacionados con la edad suelen tener su origen en múltiples factores, que contribuyen de otra manera a que en determinados pacientes la disnea sea un cuadro secundario de la exacerbación.
Por último, el dolor torácico podría reflejar una sobrecarga ventricular derecha secundaria a una hipertensión pulmonar o al empeoramiento de la isquemia miocárdica por la hipoxemia.
La discapacidad de origen no respiratorio, por ejemplo ortopédica o neurológica, puede limitar la actividad física hasta un nivel muy por debajo del umbral de disnea, obstaculizando el reconocimiento de la EPOC estable en los ancianos. En consecuencia, es necesario que el médico tenga un alto índice de sospechapara diagnosticar la EPOC en esa franja etaria.
Espirometría
La espirometría representa un papel fundamental en el proceso diagnóstico de la EPOC pero puede ser poco satisfactoria en los pacientes frágiles o debilitados. Estos factores favorecen el subdiagnóstico “epidémico” de la EPOC: casi la mitad de los pacientes con EPOC no son diagnosticados. Por lo tanto, la necesidad de cumplir con los criterios espirométricos da lugar a una selección sesgada de pacientes con diagnóstico de EPOC, debido a la exclusión automática de la mayoría de los pacientes frágiles. En efecto, los pacientes tienen que cumplir aceptablemente los criterios espirométricos (al menos 3 curvas) y por lo tanto también los criterios de repetibilidad.
En el contexto de un estudio de espirometrías en los ancianos, estudio SaRA (Salute Respiratoria nell'Anziano), 4 de 5 sujetos >64 años con o sin EPOC podrían cumplir con el criterio de aceptabilidad. El deterioro cognitivo, el mal estado físico y el nivel de educación bajo caracterizaron a los pacientes con impedimentos para la correcta ejecución de la espirometría, mientras que la edad avanzada, el género masculino y la obstrucción bronquial grave se asociaron con una repetibilidad inaceptable. Se destaca que el volumen de las espirometrías realizadas se correlacionó positivamente con la buena aceptabilidad y repetibilidad combinadas, lo que pone en evidencia que la experiencia de cada laboratorio de fisiopatología respiratoria influye en la calidad general de la espirometría.
Con el propósito de aumentar el número de ancianos con diagnóstico espirométrico se ha comenzado a utilizar el VEF6, por ej., el volumen máximo de aire espirado en cualquier momento antes de haber hecho la maniobra espiratoria forzada en el sexto segundo y haber probado repetidamente. Si el paciente no puede alcanzar una meseta espiratoria final ≥1 segundo, la CVF no es mensurable, mientras que el VEF6 sí puede ser medido. Según los autores, la relación VEF1/VF6 puede sustituir a la relación VE1/CVF.
Se ha comprobado que el VF6 tiene buenas propiedades diagnósticas para la las enfermedades respiratorias obstructivas y restrictivas. También identifica a los fumadores en riesgo de un deterioro respiratorio más rápido. La disponibilidad de estándares de referencia, aún para la población anciana, permite que el VF6 pueda ser utilizado en la práctica.
Lamentablemente, el VF6 no es una panacea: 440 de 1.971 inscriptos en el estudio SaRA no pudieron realizar la espirometría (n = 101) o alcanzar un volumen extrapolado retrógrado >150 ml, por ej., no alcanzaron la espiración explosiva requerida. Es decir, ni la CVF ni el VF6 pudieron ser medidos en 440/1.971 probandos. Por otra parte, la realización y la repetición de la CVF y el VF6 fueron defectuosas en 262 y 186 personas de las 1.531 que no realizaron bien la espirometría, respectivamente. En los pacientes mayores, las principales correlaciones de la incapacidad para lograr un VF6 fueron el deterioro cognitivo y la menor educación.
Un problema adicional para el diagnóstico de la EPOC en los ancianos, aun en los sujetos capaces de realizar la espirometría, es el criterio diagnóstico utilizado. Aunque las guías actuales usan la reducción del cociente VEF1/CVF (o CV = CV baja) como una característica para el diagnóstico de obstrucción bronquial. La reducción de la relación VEF1/CV puede utilizarse contrariamente a un valor “fijado” (usualmente 0,7) o un límite más bajo de lo normal que corresponde al percentilo 5 de la distribución teórica del parámetro en una población sana de la misma edad, género y tamaño corporal.
La primera definición es recomendada por la Global Initiative against Obstructive Lung Disease (GOLD) mientras que la última los es por la American Thoracic Society (ATS) y la European Respiratory Society (ERS). Ambas definiciones tienen sus inconvenientes.
Por un lado, el valor fijado no tiene en cuenta el VEF1 y la CV no disminuye a la misma velocidad con la edad. Como consecuencia, en los ancianos, un valor fijado tiende a diagnosticar en exceso la obstrucción bronquial en exceso.
Por otra parte, el límite inferior normal calculado mediante ecuaciones predictivas basadas en la asunción de que la variabilidad es proporcional a los valores esperados en todas las edades; su validez también depende de la disponibilidad de estándares desarrollados en una población de referencia normal, tan similar a la población estudiada como sea posible.
Ambas presunciones suelen ser irreales, especialmente en los ancianos. Se ha propuesto usar valores límite más bajos en los ancianos (0,65 y 0,67 en hombres y mujeres, respectivamente) lo que puede contrarrestar el valor de corte fijado y sesgar el límite más bajo del normal
A pesar de estas limitaciones, la espirometría sigue siendo fundamental para el diagnóstico de la EPOC y, en términos generales, para el diagnóstico de las enfermedades respiratorias a cualquier edad. Por otra parte, puede brindar información dinámica importante del atrapamiento aéreo, por ejemplo, el descenso de la CV inspiratoria relacionado con el ejercicio y provocado por el aumento del volumen espiratorio de reserva. La hiperinsuflación dinámica está muy relacionada con la disnea por lo que las intervenciones tienen que estar destinadas a limitarla y así prevenir efectivamente la disnea. Por lo tanto, la espirometría puede ser una guía terapéutica y una herramienta el diagnóstica.
Alternativas:
En los últimos tiempos se ha tratado de desarrollar métodos diagnósticos alternativos, pero no se han hallado soluciones. Una posibilidad muy interesante y promisoria está dada por la técnica de nariz electrónica que consiste en un grupo de sensores que mimetizan el epitelio olfatorio. Está basada en 6 sensores microbalanceados cubiertos con metaloporfirinas que, tras la interacción con compuestos orgánicos volátiles, son sometidos a cambios de frecuencia que pueden traducirse en una especie de gráfico de la respiración. Se ha comprobado que esta técnica tiene propiedades diagnósticas importantes en el cáncer de pulmón, el asma y la EPOC. Los resultados preliminares en pacientes ancianos con EPOC son alentadores. El método es muy fácil, barato, altamente repetible y seguro. Sin embargo, hasta el momento, la nariz electrónica debe utilizarse solamente como una herramienta de investigación. Se requieren estudios grandes para confirmar sus propiedades diagnósticas y clasificatorias.
Asma
Por último, el asma no es infrecuente en los ancianos y debe ser diferenciada de la EPOC. En esa etapa de la vida se describen 2 tipos de asma: una forma de comienzo temprano que se remonta a la juventud y es fácilmente reconocida, aun si ocurre luego de varios años, y la forma de comienzo tardío. Esta última suele ser mal catalogada como EPOC, siendo la edad avanzada y la discapacidad los principales responsables de ese error de clasificación. La eosinofilia del esputo y la necesidad frecuente de tratamiento corticosteroide despiertan la sospecha diagnóstica, pero la reversibilidad con los broncodilatadores puede ser parcial.
Por otra parte, según un análisis agrupado, un grupo de mujeres con asma no atópica de comienzo tardío, obesas y de edad avanzada presentaba reducciones moderadas del VEF1 y exacerbaciones frecuentes que requerían corticosteroides orales. En la tabla siguiente se propone un algoritmo de diagnóstico.

¿Cómo impacta la EPOC en el estado de salud de los pacientes?
La EPOC afecta el estado de salud a través de su historia natural, y más todavía cuando el VEF1 es del 50% del valor esperado. Por otra parte, aun los sujetos en los que no se ha reconocido la enfermedad sufren un deterioro evidente de la salud. La pérdida de masa muscular, la disnea, los trastornos cognitivos y afectivos, la osteoporosis y los trastornos del sueño interactúan de diversas maneras para alterar la independencia personal y la sensación subjetiva del estado de salud.
También es muy evidente que la relación entre la evolución de la EPOC y el estado de salud puede ser en alguna medida recíproca: por ejemplo, los problemas cognitivos afectan de diversas maneras el cumplimiento del tratamiento (es considerado el principal problema terapéutico en los pacientes ancianos con EPOC), mientras que los trastornos del sueño pueden fomentar el uso inapropiado de fármacos depresores de la respiración. Por otra parte, la depresión se asocia con el tabaquismo y mayor mortalidad.
Estos y otros ejemplos evidencian la posibilidad de que se produzca más el empeoramiento del estado de salud que la aceleración de la progresión de la EPOC. Por lo tanto, es muy importante interrumpir este círculo vicioso.
En el estudio SaRA, el 31% de los pacientes con EPOC tenía un buen estado de salud, como lo muestra su estado físico y cognitivo, su estado afectivo y la calidad del sueño, mientras que el 41% y el 27% tenían un deterioro moderado y grave de su estado de salud, respectivamente. Los determinantes principales fueron las variables del estado físico, como la independencia en las actividades, medida mediante la prueba de Barthel y el rendimiento físico submáximo. Inesperadamente, se halló que la concordancia entre la gravedad de la obstrucción de la vía aérea y el deterioro del estado de salud fue solo moderado; el 2,3% de los pacientes con EPOC leve tenía una alteración grave del estado de salud, mientras que el 5% de aquellos con EPOC grave tenían un estado de salud delicado.
Los factores sociales influyen en el estado de salud y, de manera especial, en el uso de los recursos para la atención sanitaria. El último también es importante para el estado de salud ya que se ha demostrado que el estado de salud disminuye luego de la estancia hospitalaria por una exacerbación de la EPOC.
En efecto, la tasa de hospitalización por exacerbación de la EPOC de las personas ancianas está inversamente relacionada el nivel de ingreso; la misma relación ha sido demostrada para otras afecciones crónicas como la diabetes mellitus y la insuficiencia cardiaca congestiva o el accidente cerebrovascular, una condición aguda profundamente arraigada en las enfermedades crónicas, pero no en la fractura de cadera. Por lo tanto, el tratamiento óptimo implica el uso de intervenciones sociales para mejorar el estado de salud.
La medición básica e instrumental de las actividades de la vida diaria, las mediciones específicas del rendimiento físico y el análisis de sus combinaciones permite verificar que la EPPOC afecta la independencia personal de una manera distintiva con respecto a otras condiciones crónicas como la insuficiencia cardíaca congestiva y la diabetes mellitus. Esta diferencia aumenta también la necesidad de atención, por ejemplo, la combinación de 3 limitaciones físicas como salir al exterior, subir o bajar escaleras y caminar por lo menos 400 metros identifica a los pacientes con una mayor duración de la exacerbación de la EPOC.

¿Cuál es el pronóstico de la EPOC?
El pronóstico general de la EPOC es malo. Se ha informado que la mortalidad a los 3 años en una población con EPOC y sin insuficiencia respiratoria u otra enfermedad grave es del 23%.
Más recientemente, los datos del estudio TORC H (Towards a Revolution in COPD Health) de pacientes con un VEF1 promedio del 44% mostraron una mortalidad del 15% en el grupo placebo. En el estudio UPLIFT (Understanding Potential Long-term Impacts on Function with Tiotropium), en el cual se enrolaron pacientes de gravedad comparable, se obtuvieron datos similares.
Estratificación
La estratificación de la gravedad de la EPOC habitualmente se basa en 3 grados de reducción del VEF1, aunque el sistema de estadificación de la guía GOLD más reciente también incluye la frecuencia de las exacerbaciones. Sin embargo, es posible que si la clasificación del riesgo en los ancianos se basa solamente en las características espiratorias el resultado sea inadecuado. La predicción de la mortalidad en una población de pacientes con EPOC y edad promedio >65 años puede hacerse mejor utilizando un índice combinado (el índice BODE) que incluye el VEF1 y el estado nutricional, la capacidad para el ejercicio y la disnea. El inconveniente de expresar el VEF1 utilizando valores predictivos también aparece cuando se estratifica el riesgo. Otras alternativas para expresar el VEF1, como el VEF1 dividido por la altura al cubo, puede ser más apropiado en la población anciana.
Heterogeniedad fenotípica
Un tema también importante que necesita ser tenido en cuenta con respecto al pronóstico es la heterogeneidad de la EPOC por sí misma. Más allá de la clásica distinción entre el fenotipo "bronquítico" y el "enfisematoso", se han descrito diferentes características distintivas─capacidad de respuesta a los broncodilatadores, frecuencia de las exacerbaciones, presencia de hipertensión pulmonar─que permiten identificar a los diferentes fenotipos de distinto pronóstico. Probablemente, la heterogeneidad del fenotipo es la responsable de la tasa tan variable de disminución del FEV1 que se observa en los pacientes con EPOC.
Comorbilidades
Por último, la comorbilidad es un factor pronóstico mayor en la EPOC de pacientes ancianos. En una muestra de 270 pacientes con una edad promedio de 67 ± 9 años y un seguimiento de hasta 3,5 años, la mortalidad estuvo más relacionada con la insuficiencia renal crónica y la enfermedad coronariaque con la disminución del VEF1 basal. Sin embargo, la edad por sí misa fue el predictor negativo principal, seguido por los signos electrocardiográficos de disfunción cardíaca derecha: la supervivencia a los 6 años fue 7% en los pacientes con una onda P por sobrecarga auricular derecha y ondas S en las derivaciones D1,D 2 yD3; el porcentaje subió al 18% en presencia de uno solo de esos signos y alcanzó el 36% en ausencia de ellos, estableciendo que los signos electrocardiográficos de hipertensión pulmonar son una manifestación de muy mal pronóstico.
La disfunción neuropsicológica, evidenciada por el copiado anormal de figuras geométricas, también contribuye a empeorar el pronóstico, posiblemente como un marcador del daño cerebral profundo, principalmente la ínsula, secundario a la hipoxemia y la hipercapnia y la consiguiente desregulación del sistema nervioso autónomo.
La mortalidad intrahospitalaria también está afectada por factores no respiratorios como la fibrilación auricular y las arritmias ventriculares. Lamentablemente, la comorbilidad, una condición que en general acompaña a la EPOC en la vejez, no ha sido sistemáticamente recogida y tomada en cuenta como un determinante pronóstico en los estudios de investigación.

¿Cuáles son los principales problemas terapéuticos en los pacientes con EPOC y cuáles son las pruebas que todavía faltan en esta población?
Muchos son los problemas que afectan la calidad del tratamiento de la EPOC en los ancianos:
1. La fuente de información de los ensayos farmacológicos se basa principalmente en criterios de selección. El ensayo TORCH utilizó 12 criterios de exclusión, el UPLIFTT 19 y el POET-COPD (Prevention of Exacerbations with Tiotropium in COPD) utilizó 22.
La comorbilidad, el deterioro cognitivo, la depresión y las limitaciones físicas que caracterizan a la EPOC en el anciano son los criterios de exclusión más utilizados. Por ejemplo, la edad media de los participantes de esos trabajos fue 65 años (40–80 años; DS 8,2) para el TORCH, 65 años (DS 8,0), para el UPLIFT, y 63 años (DS 9,0) para el POET-COPD. En consecuencia, la información basada en los ensayos “puede no ser apta" para aplicar al promedio de pacientes ancianos con EPOC que se atiende diariamente en las guardias y consultorios.
2. Los inhaladores parecen fáciles de usar pero pueden ser difíciles para los pacientes ancianos. En efecto, se requiere la coordinación y la fuerza de los músculos respiratorios para inhalar el fármaco. Se ha comprobado que el deterioro cognitivo influye notablemente en la capacidad para usar correctamente los inhaladores: un puntaje <24 en el test MMSE se asocia con un riesgo muy elevado de fracaso; aun un test de copiado del pentágono anormal, una herramienta del MMSE que evalúa la incapacidad constructiva, identifica a los pacientes que no son capaces de utilizar los inhaladores.
En presencia de deterioro cognitivo, el cumplimiento del tratamiento farmacológico y no farmacológico suele ser escaso. Las pruebas de detección como el MMSE o la evaluación neuropsicológica confirmatoria mediante el Mental Deterioration Battery o un test de memoria secundaria, por ejemplo, el test de las 15 palabras de Rey, identifican muy bien a los pacientes con EPOC en riesgo de mal cumplimiento del tratamiento.
3. La rehabilitación repetida puede retrasar mucho la declinación del estado de salud y disminuir la necesidad de atención médica, como así mejorar los trastornos del humor relacionados con la EPOC. Según estas evidencias, los pacientes deprimidos y discapacitados pueden ser incluidos y no excluidos de los programas de rehabilitación. Estos efectos beneficiosos también son evidentes en los pacientes de más edad y gravemente enfermos, pero en general, se recurre a la rehabilitación menos de lo necesario.
4. Estos pacientes tienen muchos problemas y requieren una atención destinada a disminuir su sufrimiento y a ayudar a sus familiares y cuidadores. Lamentablemente, los cuidados paliativos necesarios difieren de los cuidados paliativos para los pacientes neoplásicos; no hay mucha disponibilidad de cuidados paliativos para los pacientes respiratorios y los mismos son menos percibidos como una necesidad importante para la salud. La poca experiencia que hay al respecto muestra que la provisión domiciliaria de cuidados paliativos es bastante demandante y genera importantes problemas de organización.
5. Los pacientes ancianos con EPOC están expuestos a graves riesgos de reacciones adversas a los medicamentos debido a las sobredosis en relación con la depuración renal. En efecto, la sarcopenia, una consecuencia común de la EPOC grave atenúa el aumento de la creatinina debido a la disminución del índice de filtrado t glomerular ()FG) Por lo tanto, aun la insuficiencia renalmoderada (FG = 60–30) y grave pueden pasar desapercibidas. Este problema puede surgir en ocasión de una exacerbación aguda que requiere antibióticos o fármacos no respiratorios en forma crónica y también de algunos broncodilatadores tópicos, los cuales son depurados parcialmente por el riñón.
6. Los principales problemas en los ancianos con EPOC son la coexistencia de otras enfermedades y la polifarmacia. A menudo no está claro cuál es la guía que se debe aplicar en estos pacientes tan complejos. Por ejemplo, siempre se ha considerado que los bloqueantes ß utilizados en la insuficiencia cardíaca congestiva coexistente empeoran la obstrucción bronquial de la EPOC, mientras que actualmente están contraindicados en el asma y no en la EPOC.
Por otra parte, las comorbilidades altamente prevalentes pueden afectar enormemente la función respiratoria; por ejemplo, la osteoporosis puede provocar fracturas vertebrales y así agregar un componente restrictivo a la disfunción respiratoria.
Del mismo modo, el síndrome de apnea obstructiva del sueño, muy común pero en la vejez, tiene presentaciones atípicas y puede afectar directamente la función respiratoria. La detección y el tratamiento de las comorbilidades en los pacientes con EPOC son fundamentales y requieren la atención sistemática de los médicos.
7. Las exacerbaciones graves de la EPOC se caracterizan por el hipercatabolismo y la pérdida acelerada de masa muscular, pero en gran parte de los pacientes con EPOC también existen ciertos trastornos fenotípicos. Por lo tanto, es necesario tratar cuanto antes la exacerbación, de manera que cese la respuesta inflamatoria, brindando apoyo nutricional y rehabilitación, como partes fundamentales de dicho tratamiento.
Las intervenciones nutricionales podrían mejorar la fuerza de los músculos respiratorios y periféricos pero no los índices de función respiratoria. Como sucede en los pacientes muy frágiles y discapacitados geriátricos, valdría la pena probar un programa de intervención completo, principalmente basado en ejercicios y soporte nutricional.

¿Cómo se debe abordar a los pacientes ancianos con EPOC? ¿El enfoque realista cambia en función de la especialidad?
Mientras que en los últimos 10 años se han elaborado y difundido guías para el tratamiento de la EPOC, principalmente la GOLD, la NICE y la de ATS/ERS, actualmente la propuesta es abordar la EPOC según la especialidad médica. Se ha informado que tanto los geriatras como los neumólogos hacen un abordaje específico especializado de la EPOC mientras que los internistas se caracterizan por una gran variedad de enfoques. Curiosamente, el abordaje amplio del estado de salud es característico del enfoque geriátrico, mientras que los neumólogos se centran en la heterogeneidad fenotípica de la EPPOC.
En efecto, la evaluación amplia es común en la práctica geriátrica pero no entre los neumólogos que prestan atención a las consecuencias clínicas de la hiperinsuflación dinámica. Dado que ambos enfoques están altamente motivados por los pacientes con EPOC de edad avanzada, es preferible la combinación de elementos de ambas especialidades, con el fin de mejorar la calidad de la atención.
Lamentablemente, la mayoría de las guías más usadas (GOLD, NICE, y ATS/ERS) no se refiere a temas específicos de interés para el anciano ni destacan los cuadros característicos de la EPOC en este gran subgrupo de pacientes. En efecto, solamente en su nueva versión, la guía GOLD ha comenzado a mencionar las comorbilidades. Por otra parte, la guía ATS/ERS sobre rehabilitación trata en forma parcial estos tópicos, cuando considera la depresión y la ansiedad.

Conclusiones
La EPOC tiene una definición muy amplia para ser una enfermedad tan heterogénea. La edad avanzada aumenta esa heterogeneidad y principalmente altera su presentación típica, la cual está alterada por la comorbilidad y el poco conocimiento de los cambios que se producen con el envejecimiento que modifica la respuesta al tratamiento que ha probado ser útil en la población adulta.
Es necesario esforzarse para establecer estándares realistas válidos de la función respiratoria en la vejez como así hacer procedimientos diagnósticos adecuados para una vasta mayoría de pacientes ancianos, de manera que también las personas frágiles y discapacitadas puedan ser estudiadas para detectar y diagnosticar la EPOC. Los ensayos clínicos deben ser repensados para incluir a las personas frágiles y, por lo tanto, generar resultados del mundo real.
El abordaje global de estos pacientes debe estar basado en la experiencia y la habilidad de los diferentes especialistas para brindar un enfoque amplio de una enfermedad multifacética. Sin embargo, antes de iniciar estas acciones y a modo introductorio, hay que difundir entre la opinión pública y las autoridades políticas el concepto de que la EPOC es un problema sanitario y social grave. De hecho, dicen los autores, “las enfermedades no transmisibles crónicas como la cardiopatía isquémica o la diabetes mellitus se perciben correctamente como una carga dramática para nuestras sociedades, mientras que no sucede lo mismo con la EPOC, a pesar de la evidencia epidemiológica clara”.
El conocimiento precede e impulsa la acción: la dificultad para el diagnóstico y el tratamiento de la EPOC en los ancianos probablemente mejore solo si la enfermedad es percibida en su correcta prevalencia, complejidad y cambiante evolución en relación a edad avanzada. Los internistas, que atienden a la mayoría de los pacientes con EPOC ancianos están firmemente comprometidos para lograr este objetivo.
♦ Traducción y resumen objetivo: Dra. Marta Papponetti
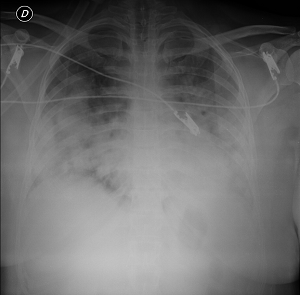
| Presentación de un caso Un hombre de 81 años con diagnóstico clínico presuntivo de enfermedad pulmonar obstructiva crónica (EPOC) y comorbilidades graves (hipertensión, angina coronaria estable, arteriopatía periférica, enfermedad renal crónica, osteoporosis, diabetes mellitus y enfermedad de Parkinson) se presentó en el departamento de emergencias con confusión de gravedad progresiva y gran somnolencia. A pesar del riesgo elevado de EPOC por la presencia de tos productiva crónica, sibilancias y disnea de esfuerzo, como así el antecedente de tabaquismo (22 paquetes/año) nunca se le había diagnosticado definitivamente la EPOC porque no permitía hacer una curva de flujo-volumen aceptable. A su ingreso, relató que desde hacía 3 días sufría dolor torácico leve y ortopnea. Antes de este proceso agudo, el paciente se sentía limitado en sus actividades básicas e instrumentales de la vida diaria, podía caminar sin ayuda y no tenía deterioro cognitivo evidente (según el puntaje del Mini Mental State Examination [MMSE] obtenido 6 meses antes: 24/30). Sin embargo, de acuerdo con sus cuidadores, usaba poco los inhaladores debido a su limitada coordinación relacionada con su rigidez extrapiramidal. En los 4 meses últimos había sido hospitalizado 2 veces por empeoramiento de la disnea y/o expectoración, además del adelgazamiento de unos 6 kg. Todos los años recibía la vacuna contra Streptococcus pneumoniae. Su tratamiento habitual consistía en: medicación inhalada triple (agonistas ß2 de acción prolongada, anticolinérgicos y corticosteroides), bloqueantes ß cardioselectivos, inhibidores de la enzima convertidora de angiotensina, ácido acetilsalicílico, metformina, glibenclamida, difosfonatos y vitamina D. Los signos vitales a su ingreso eran:
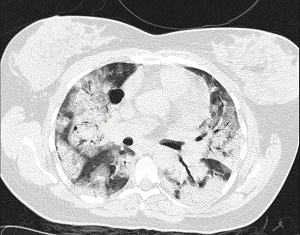
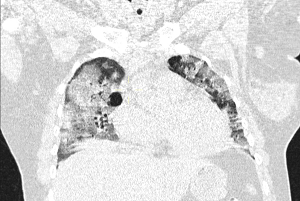
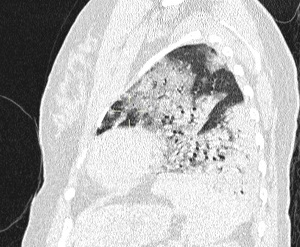
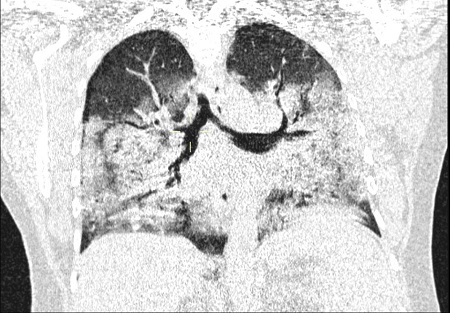
La radiografía de tórax mostraba pulmones hiperinsuflados en forma difusa y pérdida de los trazos vasculares, con hemidiafragmas aplanados, sin áreas de consolidación evidentes. Los análisis de laboratorio mostraron:
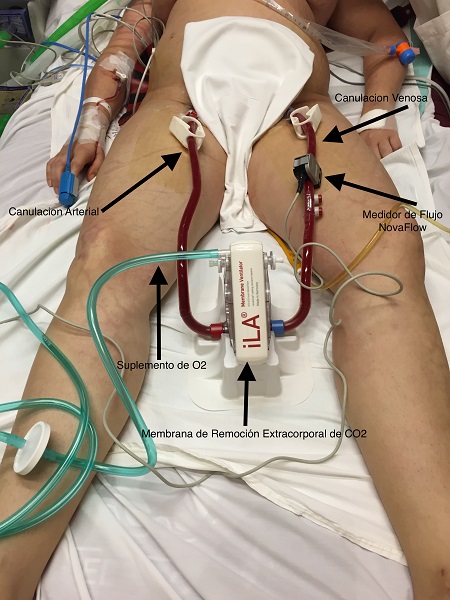
La hipoxemia, la hipercapnia y el equilibrio ácido-base volvieron a los valores normales rápidamente y el delirio desapareció. El tratamiento de sostén consistió en oxigenoterapia, aporte intravenoso de líquidos, control optimizado de la diabetes, heparina no fraccionada profiláctica y dieta personalizada. Se monitorearon muy cuidadosamente los índices respiratorios, hemodinámicos y renales. Luego de 48 horas, el paciente había recuperado íntegramente sus facultades mentales, se pudo suspender la ventilación no invasiva y se inició la rehabilitación respiratoria. Luego de un lavado farmacológico eficaz, las pruebas de función pulmonarrevelaron una obstrucción fija grave (relación VEF1/CVF (capacidad vital forzada) 43% y VEF1 34% del valor esperado, luego de la inhalación efectiva del broncodilatador) asociada a un aumento del atrapamiento aéreo (volumen residual 138% del esperado). Se realizó la evaluación geriátrica completa y se planificó un programa de atención domiciliaria. Luego del alta hospitalaria, el paciente tuvo una evaluación domiciliaria regular, en la que se reafirmó la capacitación sobre el uso correcto de los inhaladores y el reconocimiento de los primeros síntomas y signos de una exacerbación aguda. En los 6 meses siguientes, el paciente recuperó peso, tuvo menos disnea y mejoró su limitación física, sin sufrir nuevas exacerbaciones agudas de la EPOC. |
La EPOC es una enfermedad típica del envejecimiento cuya prevalencia aumenta drásticamente con la edad. En EE. UU. oscila entre el 6,6 % en el grupo de 45-54 años hasta un 12 % a partir de los 64 años. Los datos relativos de los países europeos solo se refieren a los adultos de la población general y no a la población geriátrica.
La EPOC es responsable de la mayoría de la oxigenoterapia prolongada, sobre todo en los >70 años, comparados con la población general. Estos hallazgos reflejan los efectos acumulativos del tabaquismo y la polución ambiental.
Por otra parte, el acortamiento de los telómeros, un signo distintivo del proceso de envejecimiento, también aparece en los pacientes con EPOC, así que la edad junto con la EPOC, lo promueven su ocurrencia. Se destaca que la disfunción de la telomerasa y el acortamiento acelerado de los telómeros son también comunes en las células endoteliales que participan en el proceso aterosclerótico, condiciones prototípicas relacionadas con la edad, así como con las enfermedades inmunológicas como la artritis reumatoidea, las cuales están estrictamente relacionadas con la edad. Parece haber una base biológica clara que subyace en la evidencia epidemiológica, aunque el vínculo entre la EPOC y la telomerasa defectuosa debe ser distinguido de los efectos de las infecciones previas, como la infección por Citomegalovirus.
Hay otras similitudes entre el envejecimiento del pulmón y el pulmón de la EPOC que son dignas de mención:
En el envejecimiento normal, la capacidad vital declina anualmente 10-20 ml, mientras que en los pacientes con EPOC la declinación es de unos 30 ml; el volumen residual aumenta tanto en el envejecimiento normal como en el pulmón de la EPOC. Por otra parte, en las personas mayores hay una pérdida de la elasticidad, la depuración mucociliar, la inmunidad de la mucosa y la reserva vascular, más acentuada en la EPOC. A pesar de la estrecha relación con la edad, la prevalencia de la EPOC en los ancianos no se conoce por completo. En efecto, tanto los cambios relacionados con la edad que aparecen en la presentación clínica de la EPOC como el enmascaramiento derivado de las comorbilidades, sumado a los problemas para ejecutar la espirometría contribuyen a obstaculizar el diagnóstico de la enfermedad en la población de edad avanzada.
¿Por qué es difícil el diagnóstico de la EPOC en la población de edad avanzada?
"Casi la mitad de los pacientes con EPOC no son diagnosticados"
La EPOC raramente se presenta sola en los pacientes ancianos. La comorbilidad y la discapacidad de varios órganos contribuyen a la dificultad para reconocer la EPOC. Por otra parte, los trastornos cognitivos, principalmente de la memoria verbal y la capacidad constructiva, como así la depresión pueden predominar en el escenario clínico de los sujetos con hipoxemia e hipercapnia.Aun las exacerbaciones graves de la EPOC pueden ser reconocidas tardíamente debido a una presentación atípica. En efecto, a diferencia de la triada clásica de disnea, tos y fiebre, la EPOC también puede presentarse con debilidad muscular, vértigo, confusión y edema de las piernas, cuadros que reflejan una hipoxemia grave y que son característicos de las presentaciones atípicas, en ocasiones también el delirio puede ser la principal manifestación.
El aumento del umbral de disnea y la discapacidad física relacionados con la edad suelen tener su origen en múltiples factores, que contribuyen de otra manera a que en determinados pacientes la disnea sea un cuadro secundario de la exacerbación.
Por último, el dolor torácico podría reflejar una sobrecarga ventricular derecha secundaria a una hipertensión pulmonar o al empeoramiento de la isquemia miocárdica por la hipoxemia.
La discapacidad de origen no respiratorio, por ejemplo ortopédica o neurológica, puede limitar la actividad física hasta un nivel muy por debajo del umbral de disnea, obstaculizando el reconocimiento de la EPOC estable en los ancianos. En consecuencia, es necesario que el médico tenga un alto índice de sospechapara diagnosticar la EPOC en esa franja etaria.
Espirometría
La espirometría representa un papel fundamental en el proceso diagnóstico de la EPOC pero puede ser poco satisfactoria en los pacientes frágiles o debilitados. Estos factores favorecen el subdiagnóstico “epidémico” de la EPOC: casi la mitad de los pacientes con EPOC no son diagnosticados. Por lo tanto, la necesidad de cumplir con los criterios espirométricos da lugar a una selección sesgada de pacientes con diagnóstico de EPOC, debido a la exclusión automática de la mayoría de los pacientes frágiles. En efecto, los pacientes tienen que cumplir aceptablemente los criterios espirométricos (al menos 3 curvas) y por lo tanto también los criterios de repetibilidad.
En el contexto de un estudio de espirometrías en los ancianos, estudio SaRA (Salute Respiratoria nell'Anziano), 4 de 5 sujetos >64 años con o sin EPOC podrían cumplir con el criterio de aceptabilidad. El deterioro cognitivo, el mal estado físico y el nivel de educación bajo caracterizaron a los pacientes con impedimentos para la correcta ejecución de la espirometría, mientras que la edad avanzada, el género masculino y la obstrucción bronquial grave se asociaron con una repetibilidad inaceptable. Se destaca que el volumen de las espirometrías realizadas se correlacionó positivamente con la buena aceptabilidad y repetibilidad combinadas, lo que pone en evidencia que la experiencia de cada laboratorio de fisiopatología respiratoria influye en la calidad general de la espirometría.
Con el propósito de aumentar el número de ancianos con diagnóstico espirométrico se ha comenzado a utilizar el VEF6, por ej., el volumen máximo de aire espirado en cualquier momento antes de haber hecho la maniobra espiratoria forzada en el sexto segundo y haber probado repetidamente. Si el paciente no puede alcanzar una meseta espiratoria final ≥1 segundo, la CVF no es mensurable, mientras que el VEF6 sí puede ser medido. Según los autores, la relación VEF1/VF6 puede sustituir a la relación VE1/CVF.
Se ha comprobado que el VF6 tiene buenas propiedades diagnósticas para la las enfermedades respiratorias obstructivas y restrictivas. También identifica a los fumadores en riesgo de un deterioro respiratorio más rápido. La disponibilidad de estándares de referencia, aún para la población anciana, permite que el VF6 pueda ser utilizado en la práctica.
Lamentablemente, el VF6 no es una panacea: 440 de 1.971 inscriptos en el estudio SaRA no pudieron realizar la espirometría (n = 101) o alcanzar un volumen extrapolado retrógrado >150 ml, por ej., no alcanzaron la espiración explosiva requerida. Es decir, ni la CVF ni el VF6 pudieron ser medidos en 440/1.971 probandos. Por otra parte, la realización y la repetición de la CVF y el VF6 fueron defectuosas en 262 y 186 personas de las 1.531 que no realizaron bien la espirometría, respectivamente. En los pacientes mayores, las principales correlaciones de la incapacidad para lograr un VF6 fueron el deterioro cognitivo y la menor educación.
Un problema adicional para el diagnóstico de la EPOC en los ancianos, aun en los sujetos capaces de realizar la espirometría, es el criterio diagnóstico utilizado. Aunque las guías actuales usan la reducción del cociente VEF1/CVF (o CV = CV baja) como una característica para el diagnóstico de obstrucción bronquial. La reducción de la relación VEF1/CV puede utilizarse contrariamente a un valor “fijado” (usualmente 0,7) o un límite más bajo de lo normal que corresponde al percentilo 5 de la distribución teórica del parámetro en una población sana de la misma edad, género y tamaño corporal.
La primera definición es recomendada por la Global Initiative against Obstructive Lung Disease (GOLD) mientras que la última los es por la American Thoracic Society (ATS) y la European Respiratory Society (ERS). Ambas definiciones tienen sus inconvenientes.
Por un lado, el valor fijado no tiene en cuenta el VEF1 y la CV no disminuye a la misma velocidad con la edad. Como consecuencia, en los ancianos, un valor fijado tiende a diagnosticar en exceso la obstrucción bronquial en exceso.
Por otra parte, el límite inferior normal calculado mediante ecuaciones predictivas basadas en la asunción de que la variabilidad es proporcional a los valores esperados en todas las edades; su validez también depende de la disponibilidad de estándares desarrollados en una población de referencia normal, tan similar a la población estudiada como sea posible.
Ambas presunciones suelen ser irreales, especialmente en los ancianos. Se ha propuesto usar valores límite más bajos en los ancianos (0,65 y 0,67 en hombres y mujeres, respectivamente) lo que puede contrarrestar el valor de corte fijado y sesgar el límite más bajo del normal
A pesar de estas limitaciones, la espirometría sigue siendo fundamental para el diagnóstico de la EPOC y, en términos generales, para el diagnóstico de las enfermedades respiratorias a cualquier edad. Por otra parte, puede brindar información dinámica importante del atrapamiento aéreo, por ejemplo, el descenso de la CV inspiratoria relacionado con el ejercicio y provocado por el aumento del volumen espiratorio de reserva. La hiperinsuflación dinámica está muy relacionada con la disnea por lo que las intervenciones tienen que estar destinadas a limitarla y así prevenir efectivamente la disnea. Por lo tanto, la espirometría puede ser una guía terapéutica y una herramienta el diagnóstica.
Alternativas:
En los últimos tiempos se ha tratado de desarrollar métodos diagnósticos alternativos, pero no se han hallado soluciones. Una posibilidad muy interesante y promisoria está dada por la técnica de nariz electrónica que consiste en un grupo de sensores que mimetizan el epitelio olfatorio. Está basada en 6 sensores microbalanceados cubiertos con metaloporfirinas que, tras la interacción con compuestos orgánicos volátiles, son sometidos a cambios de frecuencia que pueden traducirse en una especie de gráfico de la respiración. Se ha comprobado que esta técnica tiene propiedades diagnósticas importantes en el cáncer de pulmón, el asma y la EPOC. Los resultados preliminares en pacientes ancianos con EPOC son alentadores. El método es muy fácil, barato, altamente repetible y seguro. Sin embargo, hasta el momento, la nariz electrónica debe utilizarse solamente como una herramienta de investigación. Se requieren estudios grandes para confirmar sus propiedades diagnósticas y clasificatorias.
Asma
Por último, el asma no es infrecuente en los ancianos y debe ser diferenciada de la EPOC. En esa etapa de la vida se describen 2 tipos de asma: una forma de comienzo temprano que se remonta a la juventud y es fácilmente reconocida, aun si ocurre luego de varios años, y la forma de comienzo tardío. Esta última suele ser mal catalogada como EPOC, siendo la edad avanzada y la discapacidad los principales responsables de ese error de clasificación. La eosinofilia del esputo y la necesidad frecuente de tratamiento corticosteroide despiertan la sospecha diagnóstica, pero la reversibilidad con los broncodilatadores puede ser parcial.
Por otra parte, según un análisis agrupado, un grupo de mujeres con asma no atópica de comienzo tardío, obesas y de edad avanzada presentaba reducciones moderadas del VEF1 y exacerbaciones frecuentes que requerían corticosteroides orales. En la tabla siguiente se propone un algoritmo de diagnóstico.
¿Cómo impacta la EPOC en el estado de salud de los pacientes?
La EPOC afecta el estado de salud a través de su historia natural, y más todavía cuando el VEF1 es del 50% del valor esperado. Por otra parte, aun los sujetos en los que no se ha reconocido la enfermedad sufren un deterioro evidente de la salud. La pérdida de masa muscular, la disnea, los trastornos cognitivos y afectivos, la osteoporosis y los trastornos del sueño interactúan de diversas maneras para alterar la independencia personal y la sensación subjetiva del estado de salud.
También es muy evidente que la relación entre la evolución de la EPOC y el estado de salud puede ser en alguna medida recíproca: por ejemplo, los problemas cognitivos afectan de diversas maneras el cumplimiento del tratamiento (es considerado el principal problema terapéutico en los pacientes ancianos con EPOC), mientras que los trastornos del sueño pueden fomentar el uso inapropiado de fármacos depresores de la respiración. Por otra parte, la depresión se asocia con el tabaquismo y mayor mortalidad.
Estos y otros ejemplos evidencian la posibilidad de que se produzca más el empeoramiento del estado de salud que la aceleración de la progresión de la EPOC. Por lo tanto, es muy importante interrumpir este círculo vicioso.
En el estudio SaRA, el 31% de los pacientes con EPOC tenía un buen estado de salud, como lo muestra su estado físico y cognitivo, su estado afectivo y la calidad del sueño, mientras que el 41% y el 27% tenían un deterioro moderado y grave de su estado de salud, respectivamente. Los determinantes principales fueron las variables del estado físico, como la independencia en las actividades, medida mediante la prueba de Barthel y el rendimiento físico submáximo. Inesperadamente, se halló que la concordancia entre la gravedad de la obstrucción de la vía aérea y el deterioro del estado de salud fue solo moderado; el 2,3% de los pacientes con EPOC leve tenía una alteración grave del estado de salud, mientras que el 5% de aquellos con EPOC grave tenían un estado de salud delicado.
"La tasa de hospitalización por exacerbación de la EPOC de las personas ancianas está inversamente relacionada el nivel de ingresos"
Estos hallazgos despiertan inquietud en cuanto a la excesiva simplificación de la relación entre la obstrucción bronquial y el estado de salud. Tanto la variabilidad fenotípica como la comorbilidad afectan de distintas maneras el estado de salud. Por ejemplo, la hiperinsuflación dinámica, el fenómeno del atrapamiento aéreo dependiente del ejercicio, se asoció con disnea importante y luego, con la limitación física.Los factores sociales influyen en el estado de salud y, de manera especial, en el uso de los recursos para la atención sanitaria. El último también es importante para el estado de salud ya que se ha demostrado que el estado de salud disminuye luego de la estancia hospitalaria por una exacerbación de la EPOC.
En efecto, la tasa de hospitalización por exacerbación de la EPOC de las personas ancianas está inversamente relacionada el nivel de ingreso; la misma relación ha sido demostrada para otras afecciones crónicas como la diabetes mellitus y la insuficiencia cardiaca congestiva o el accidente cerebrovascular, una condición aguda profundamente arraigada en las enfermedades crónicas, pero no en la fractura de cadera. Por lo tanto, el tratamiento óptimo implica el uso de intervenciones sociales para mejorar el estado de salud.
La medición básica e instrumental de las actividades de la vida diaria, las mediciones específicas del rendimiento físico y el análisis de sus combinaciones permite verificar que la EPPOC afecta la independencia personal de una manera distintiva con respecto a otras condiciones crónicas como la insuficiencia cardíaca congestiva y la diabetes mellitus. Esta diferencia aumenta también la necesidad de atención, por ejemplo, la combinación de 3 limitaciones físicas como salir al exterior, subir o bajar escaleras y caminar por lo menos 400 metros identifica a los pacientes con una mayor duración de la exacerbación de la EPOC.
¿Cuál es el pronóstico de la EPOC?
El pronóstico general de la EPOC es malo. Se ha informado que la mortalidad a los 3 años en una población con EPOC y sin insuficiencia respiratoria u otra enfermedad grave es del 23%.
Más recientemente, los datos del estudio TORC H (Towards a Revolution in COPD Health) de pacientes con un VEF1 promedio del 44% mostraron una mortalidad del 15% en el grupo placebo. En el estudio UPLIFT (Understanding Potential Long-term Impacts on Function with Tiotropium), en el cual se enrolaron pacientes de gravedad comparable, se obtuvieron datos similares.
Estratificación
La estratificación de la gravedad de la EPOC habitualmente se basa en 3 grados de reducción del VEF1, aunque el sistema de estadificación de la guía GOLD más reciente también incluye la frecuencia de las exacerbaciones. Sin embargo, es posible que si la clasificación del riesgo en los ancianos se basa solamente en las características espiratorias el resultado sea inadecuado. La predicción de la mortalidad en una población de pacientes con EPOC y edad promedio >65 años puede hacerse mejor utilizando un índice combinado (el índice BODE) que incluye el VEF1 y el estado nutricional, la capacidad para el ejercicio y la disnea. El inconveniente de expresar el VEF1 utilizando valores predictivos también aparece cuando se estratifica el riesgo. Otras alternativas para expresar el VEF1, como el VEF1 dividido por la altura al cubo, puede ser más apropiado en la población anciana.
Heterogeniedad fenotípica
Un tema también importante que necesita ser tenido en cuenta con respecto al pronóstico es la heterogeneidad de la EPOC por sí misma. Más allá de la clásica distinción entre el fenotipo "bronquítico" y el "enfisematoso", se han descrito diferentes características distintivas─capacidad de respuesta a los broncodilatadores, frecuencia de las exacerbaciones, presencia de hipertensión pulmonar─que permiten identificar a los diferentes fenotipos de distinto pronóstico. Probablemente, la heterogeneidad del fenotipo es la responsable de la tasa tan variable de disminución del FEV1 que se observa en los pacientes con EPOC.
Comorbilidades
Por último, la comorbilidad es un factor pronóstico mayor en la EPOC de pacientes ancianos. En una muestra de 270 pacientes con una edad promedio de 67 ± 9 años y un seguimiento de hasta 3,5 años, la mortalidad estuvo más relacionada con la insuficiencia renal crónica y la enfermedad coronariaque con la disminución del VEF1 basal. Sin embargo, la edad por sí misa fue el predictor negativo principal, seguido por los signos electrocardiográficos de disfunción cardíaca derecha: la supervivencia a los 6 años fue 7% en los pacientes con una onda P por sobrecarga auricular derecha y ondas S en las derivaciones D1,D 2 yD3; el porcentaje subió al 18% en presencia de uno solo de esos signos y alcanzó el 36% en ausencia de ellos, estableciendo que los signos electrocardiográficos de hipertensión pulmonar son una manifestación de muy mal pronóstico.
La disfunción neuropsicológica, evidenciada por el copiado anormal de figuras geométricas, también contribuye a empeorar el pronóstico, posiblemente como un marcador del daño cerebral profundo, principalmente la ínsula, secundario a la hipoxemia y la hipercapnia y la consiguiente desregulación del sistema nervioso autónomo.
La mortalidad intrahospitalaria también está afectada por factores no respiratorios como la fibrilación auricular y las arritmias ventriculares. Lamentablemente, la comorbilidad, una condición que en general acompaña a la EPOC en la vejez, no ha sido sistemáticamente recogida y tomada en cuenta como un determinante pronóstico en los estudios de investigación.
¿Cuáles son los principales problemas terapéuticos en los pacientes con EPOC y cuáles son las pruebas que todavía faltan en esta población?
Muchos son los problemas que afectan la calidad del tratamiento de la EPOC en los ancianos:
1. La fuente de información de los ensayos farmacológicos se basa principalmente en criterios de selección. El ensayo TORCH utilizó 12 criterios de exclusión, el UPLIFTT 19 y el POET-COPD (Prevention of Exacerbations with Tiotropium in COPD) utilizó 22.
La comorbilidad, el deterioro cognitivo, la depresión y las limitaciones físicas que caracterizan a la EPOC en el anciano son los criterios de exclusión más utilizados. Por ejemplo, la edad media de los participantes de esos trabajos fue 65 años (40–80 años; DS 8,2) para el TORCH, 65 años (DS 8,0), para el UPLIFT, y 63 años (DS 9,0) para el POET-COPD. En consecuencia, la información basada en los ensayos “puede no ser apta" para aplicar al promedio de pacientes ancianos con EPOC que se atiende diariamente en las guardias y consultorios.
2. Los inhaladores parecen fáciles de usar pero pueden ser difíciles para los pacientes ancianos. En efecto, se requiere la coordinación y la fuerza de los músculos respiratorios para inhalar el fármaco. Se ha comprobado que el deterioro cognitivo influye notablemente en la capacidad para usar correctamente los inhaladores: un puntaje <24 en el test MMSE se asocia con un riesgo muy elevado de fracaso; aun un test de copiado del pentágono anormal, una herramienta del MMSE que evalúa la incapacidad constructiva, identifica a los pacientes que no son capaces de utilizar los inhaladores.
En presencia de deterioro cognitivo, el cumplimiento del tratamiento farmacológico y no farmacológico suele ser escaso. Las pruebas de detección como el MMSE o la evaluación neuropsicológica confirmatoria mediante el Mental Deterioration Battery o un test de memoria secundaria, por ejemplo, el test de las 15 palabras de Rey, identifican muy bien a los pacientes con EPOC en riesgo de mal cumplimiento del tratamiento.
3. La rehabilitación repetida puede retrasar mucho la declinación del estado de salud y disminuir la necesidad de atención médica, como así mejorar los trastornos del humor relacionados con la EPOC. Según estas evidencias, los pacientes deprimidos y discapacitados pueden ser incluidos y no excluidos de los programas de rehabilitación. Estos efectos beneficiosos también son evidentes en los pacientes de más edad y gravemente enfermos, pero en general, se recurre a la rehabilitación menos de lo necesario.
4. Estos pacientes tienen muchos problemas y requieren una atención destinada a disminuir su sufrimiento y a ayudar a sus familiares y cuidadores. Lamentablemente, los cuidados paliativos necesarios difieren de los cuidados paliativos para los pacientes neoplásicos; no hay mucha disponibilidad de cuidados paliativos para los pacientes respiratorios y los mismos son menos percibidos como una necesidad importante para la salud. La poca experiencia que hay al respecto muestra que la provisión domiciliaria de cuidados paliativos es bastante demandante y genera importantes problemas de organización.
5. Los pacientes ancianos con EPOC están expuestos a graves riesgos de reacciones adversas a los medicamentos debido a las sobredosis en relación con la depuración renal. En efecto, la sarcopenia, una consecuencia común de la EPOC grave atenúa el aumento de la creatinina debido a la disminución del índice de filtrado t glomerular ()FG) Por lo tanto, aun la insuficiencia renalmoderada (FG = 60–30) y grave pueden pasar desapercibidas. Este problema puede surgir en ocasión de una exacerbación aguda que requiere antibióticos o fármacos no respiratorios en forma crónica y también de algunos broncodilatadores tópicos, los cuales son depurados parcialmente por el riñón.
6. Los principales problemas en los ancianos con EPOC son la coexistencia de otras enfermedades y la polifarmacia. A menudo no está claro cuál es la guía que se debe aplicar en estos pacientes tan complejos. Por ejemplo, siempre se ha considerado que los bloqueantes ß utilizados en la insuficiencia cardíaca congestiva coexistente empeoran la obstrucción bronquial de la EPOC, mientras que actualmente están contraindicados en el asma y no en la EPOC.
Por otra parte, las comorbilidades altamente prevalentes pueden afectar enormemente la función respiratoria; por ejemplo, la osteoporosis puede provocar fracturas vertebrales y así agregar un componente restrictivo a la disfunción respiratoria.
Del mismo modo, el síndrome de apnea obstructiva del sueño, muy común pero en la vejez, tiene presentaciones atípicas y puede afectar directamente la función respiratoria. La detección y el tratamiento de las comorbilidades en los pacientes con EPOC son fundamentales y requieren la atención sistemática de los médicos.
7. Las exacerbaciones graves de la EPOC se caracterizan por el hipercatabolismo y la pérdida acelerada de masa muscular, pero en gran parte de los pacientes con EPOC también existen ciertos trastornos fenotípicos. Por lo tanto, es necesario tratar cuanto antes la exacerbación, de manera que cese la respuesta inflamatoria, brindando apoyo nutricional y rehabilitación, como partes fundamentales de dicho tratamiento.
Las intervenciones nutricionales podrían mejorar la fuerza de los músculos respiratorios y periféricos pero no los índices de función respiratoria. Como sucede en los pacientes muy frágiles y discapacitados geriátricos, valdría la pena probar un programa de intervención completo, principalmente basado en ejercicios y soporte nutricional.
¿Cómo se debe abordar a los pacientes ancianos con EPOC? ¿El enfoque realista cambia en función de la especialidad?
Mientras que en los últimos 10 años se han elaborado y difundido guías para el tratamiento de la EPOC, principalmente la GOLD, la NICE y la de ATS/ERS, actualmente la propuesta es abordar la EPOC según la especialidad médica. Se ha informado que tanto los geriatras como los neumólogos hacen un abordaje específico especializado de la EPOC mientras que los internistas se caracterizan por una gran variedad de enfoques. Curiosamente, el abordaje amplio del estado de salud es característico del enfoque geriátrico, mientras que los neumólogos se centran en la heterogeneidad fenotípica de la EPPOC.
En efecto, la evaluación amplia es común en la práctica geriátrica pero no entre los neumólogos que prestan atención a las consecuencias clínicas de la hiperinsuflación dinámica. Dado que ambos enfoques están altamente motivados por los pacientes con EPOC de edad avanzada, es preferible la combinación de elementos de ambas especialidades, con el fin de mejorar la calidad de la atención.
Lamentablemente, la mayoría de las guías más usadas (GOLD, NICE, y ATS/ERS) no se refiere a temas específicos de interés para el anciano ni destacan los cuadros característicos de la EPOC en este gran subgrupo de pacientes. En efecto, solamente en su nueva versión, la guía GOLD ha comenzado a mencionar las comorbilidades. Por otra parte, la guía ATS/ERS sobre rehabilitación trata en forma parcial estos tópicos, cuando considera la depresión y la ansiedad.
Conclusiones
La EPOC tiene una definición muy amplia para ser una enfermedad tan heterogénea. La edad avanzada aumenta esa heterogeneidad y principalmente altera su presentación típica, la cual está alterada por la comorbilidad y el poco conocimiento de los cambios que se producen con el envejecimiento que modifica la respuesta al tratamiento que ha probado ser útil en la población adulta.
Es necesario esforzarse para establecer estándares realistas válidos de la función respiratoria en la vejez como así hacer procedimientos diagnósticos adecuados para una vasta mayoría de pacientes ancianos, de manera que también las personas frágiles y discapacitadas puedan ser estudiadas para detectar y diagnosticar la EPOC. Los ensayos clínicos deben ser repensados para incluir a las personas frágiles y, por lo tanto, generar resultados del mundo real.
El abordaje global de estos pacientes debe estar basado en la experiencia y la habilidad de los diferentes especialistas para brindar un enfoque amplio de una enfermedad multifacética. Sin embargo, antes de iniciar estas acciones y a modo introductorio, hay que difundir entre la opinión pública y las autoridades políticas el concepto de que la EPOC es un problema sanitario y social grave. De hecho, dicen los autores, “las enfermedades no transmisibles crónicas como la cardiopatía isquémica o la diabetes mellitus se perciben correctamente como una carga dramática para nuestras sociedades, mientras que no sucede lo mismo con la EPOC, a pesar de la evidencia epidemiológica clara”.
El conocimiento precede e impulsa la acción: la dificultad para el diagnóstico y el tratamiento de la EPOC en los ancianos probablemente mejore solo si la enfermedad es percibida en su correcta prevalencia, complejidad y cambiante evolución en relación a edad avanzada. Los internistas, que atienden a la mayoría de los pacientes con EPOC ancianos están firmemente comprometidos para lograr este objetivo.
♦ Traducción y resumen objetivo: Dra. Marta Papponetti