Remoción extracorporal de CO2 en Síndrome de Distres Respiratorio Agudo severoAutor: Dr. Federico Acharta; Dr. Agñel Ramos; Lic. Jose Robles; Dr. Carlos Lovesio. Sanatorio Parque, Rosario, Santa Fe, Argentina IntraMed Journal Vol 6, No 1Presentación de un caso de SDRA severo por virus Influenza de muy difícil manejo ventilatorio que gracias a la utilización de técnicas de remoción de CO2 y manejo ventilatorio ultra protectivo permitió la resolución exitosa del cuadro
| Resumen: Objetivo: reportar un caso de Síndrome de Distres Respiratorio Agudo (SDRA) severo por virus Influenza de muy difícil manejo ventilatorio que gracias a la utilización de técnicas de remoción de Dióxido de Carbono (CO2) extracorporales (de uso poco frecuente en nuestro medio) y manejo ventilatorio ultra protectivo permitió la resolución exitosa del cuadro. Método: mujer de 33 años de edad con antecedentes de trombofilia sintomática en estudio, hipotiroidismo y asma que ingresa a la Unidad de Terapia Intensiva por cuadro de insuficiencia respiratoria severa secundaria a SDRA por Virus Influenza. Requiere asistencia ventilatoria mecánica y remoción de CO2 extracorporal. Resultados: lenta recuperación con resolución exitosa del cuadro que permitió el alta sanatorial en buenas condiciones clínicas y sin secuelas funcionales. Conclusiones: se deben tener en cuenta técnicas extracorporales de remoción de CO2 en casos de SDRA severos, que permitan utilizar estrategias ventilatorias ultra protectivas para mejor manejo de la hipercapnia que puede aparecer con el uso de estas modalidades ventilatorias. |
El Síndrome de Distres Respiratorio Agudo (SDRA) es un cuadro grave que se ve de forma frecuentemente en las Unidades de Terapia Intensiva (UTI) de todo el mundo.
Desde la epidemia de Gripe A en el año 2009 en Argentina, y gracias a la masificación de test serológicos para la detección del Virus Influenza (y sus variados serotipos) en pacientes críticos se logran diagnosticar con mayor frecuencia cuadros respiratorios provocados por este virus entre los pacientes que ingresan a UTI.1, 2, 3&
La incidencia, morbilidad y mortalidad de esta epidemia en la Argentina no difiere de la de otros países y no a demostrado grandes variaciones en los brotes estacionales de los últimos años, en gran parte sustentado por las campañas de vacunación masiva en grupos de riesgo.
Aun así, en un grado variable, de acuerdo a las cepas prevalentes y las condiciones clínicas previas de los pacientes, estos cuadros de SDRA presentan criterios de severidad que obligan a buscar técnicas asociadas de soporte vital respiratorio para el adecuado tratamiento del cuadro.4, 5&
En este caso clínico en particular la paciente presentaba una hipoxemia marcada asociada a hipercapnia severa que hacia dificultosa la implementación de técnicas protectivas/ultraprotectivas de asistencia mecánica respiratoria (AMR).
Dadas estas características particulares la utilización de técnicas de remoción extracorporal de CO2 cobran vital importancia en el manejo ventilatorio del paciente.
El SDRA representa una respuesta típica del pulmón a diversas noxas que llevan a una serie variable de fases de respuesta o defensa.
► Caso Clínico
Paciente de 33 años de edad, de sexo femenino, con antecedentes de trombofilia en estudio(6), asma e hipotiroidismo que consulta por cuadro de síndrome febril con síntomas respiratorios (tos seca, disnea progresiva, taquipnea) de 7 días de evolución bajo tratamiento antibiótico ambulatorio con amoxicilina ácido clavulánico en paciente no vacunada contra virus Influenza.
Al ingreso paciente febril, hemodinamicamente estable con insuficiencia respiratoria severa disnea grado IV. Imágenes exudativas bilaterales a predominio bibasal compatibles con SDRA en la Radiografía de Tórax y en la Tomografía MultiSlice de Tórax.
(Imagen 1. Radiografía de Tórax) (Imagen 2. (a, b, c, d) Tomografía MultiSlice de Tórax)
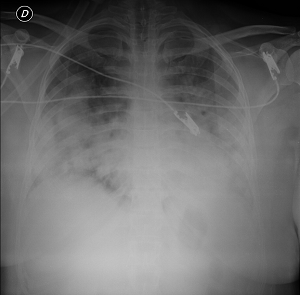 | 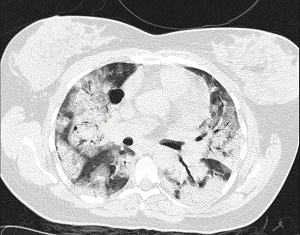 |
| Imagen 1. Radiografía Tórax Frente Al Ingreso | Imagen 2.a Tomografía MultiSlice de Tórax Al ingreso. Corte Axial |
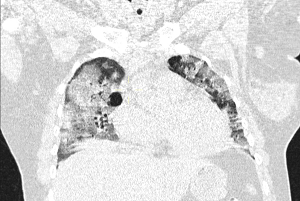 | 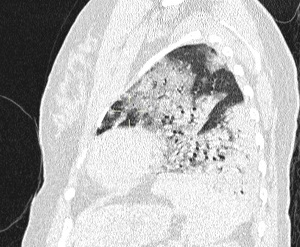 |
| Imagen 2.b Tomografía MultiSlice de Tórax Al Ingreso. Corte Coronal | Imagen 2.c Tomografía MultiSlice de Tórax Al Ingreso. Corte Parasagital |
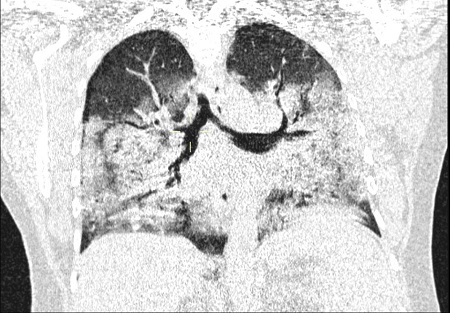
Imagen 2.d Tomografia MultiSlice de Torax Al Ingreso Corte Coronal
La paciente presenta una mala evolución clínica con rápido requerimiento de Asistencia Mecánica Respiratoria (AMR) y desarrollo progresivo de una marcada hipoxemia con hipercapnia severa que dificulta la AMR aun con la utilización de estrategias protectivas (Volumen tidal < 6 ml./kg. peso ideal). Se inicia tratamiento antibiótico endovenoso con meropenem y tratamiento antiviral con oseltamivir por alta sospecha de infección por virus influenza.
(Tabla 2. Progresión de controles de EAB en primeras 24 horas de Internacion)
LABORATORIO al INGRESO
|
Resultado
|
Hematocrito (%)
|
40
|
Globulos Blancos (elem/mm3)
|
3700
|
Neutrofilos (%)
|
85
|
Linfocitos (%)
|
11
|
Plaquetas (elem/mm3)
|
80000
|
Tiempo de Protrombina (seg.)
|
13.9
|
| KPTT (seg.) |
37
|
Uremia (mg/dl)
|
38
|
Creatininemia (mg/dl)
|
0.96
|
Natremia (mEq/L)
|
132
|
Potasemia(mEq/L)
|
3.06
|
Calcemia (mg/dl)
|
8.4
|
Magnesemia (mg/dl)
|
1.82
|
Lactato Dehidrogenasa (LDH U/L)
|
1500
|
Ph
|
7.49
|
PaO2 (mm. Hg)
|
44.6
|
PaCO2 (mm. Hg)
|
33
|
Exceso de Base
|
2
|
Saturacion Arterial de O2 (%)
|
85
|
Bicarbonato (mg/ml)
|
24.8
|
Tabla 1. Laboratorio de Ingreso
| Fecha | 31/5/16 | 31/5/16 | 31/5/16 | 31/5/16 | 1/6/16 |
| Hora | 20:00 | 21:00 | 21:30 | 23:30 | 3:00 |
| Ph | 7.49 | 7.33 | 7.28 | 7.29 | 7.29 |
| PaCO2 (mmHg) | 33 | 44 | 57 | 54.3 | 56 |
| PaO2 (mmHg) | 44.6 | 46.7 | 73.7 | 58 | 66 |
| Exceso de Base | 2.1 | -3 | -2 | -1 | -1 |
| Bicarbonato (mEq/L) | 24.8 | 23 | 26.2 | 26 | 25 |
| Sat.O2 (%) | 85 | 78 | 92.1 | 86 | 89 |
| PAFI | 89.2 | 93.4 | 113 | 80 | 66 |
Tabla 2. Progresión Controles EAB en las primeras 24 horas de Internación.
A las 24 horas del ingreso la paciente evoluciona hemodinamicamente estable, persistentemente febril y con falla respiratoria severa. Se confirma mediante serología la etiología viral por Virus Influenza del cuadro de SDRA. (Informe Serológico Gen M2 Influenza A Universal Detectable Gen H1 Nueva Influenza A Detectable).Por la mala evolución de su cuadro respiratorio asociado a la adecuada estabilidad hemodinámica de la paciente se decide iniciar a 24 horas de su ingreso la remoción extracorporal de CO2 mediante membrana extracorpórea con control de flujo arterio venoso. (iLA Membrane VentilatorTM NovalungTMcon Control de Flujo Arterio Venoso por NovaFlowTM), el control de ventilación pulmonar regional mediante equipo PulmovistaTM V500 (Imagen 3. Sistema iLA Membrane Ventilator NovalungTM) y control de presiones Intra Torácica mediante catéter intraesofágico.
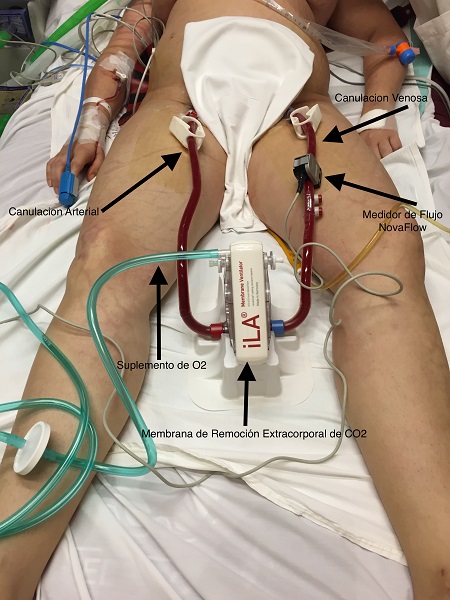
Imagen 3. iLATM Membrane Ventilator NovalungTM
PLANILLA DE CONTROL
REMOCION EXTRACORPORAL DE CO2 iLA Membrane Ventilator Novalung | ||||||||||||
Paciente:------------
| ||||||||||||
Edad: 33 años
| ||||||||||||
Altura: 166 centimetros
| ||||||||||||
Peso: 57 Kilogramos
| ||||||||||||
Fecha
|
1/6
|
1/6
|
1/6
|
1/6
|
1/6
|
2/6
|
2/6
|
2/6
|
2/6
|
2/6
|
2/6
|
2/6
|
Hora
| 19:45 |
20:05
|
20:15
|
22:00
|
23:00
|
0:00
|
1:00
|
4:00
|
5:00
|
6:00
|
8:00
|
11:00
|
Flujo O2 (litros/minutos)
|
1
|
2
|
3
|
4
|
5
|
6
|
6
|
6
|
6
|
6
|
9
|
12
|
Flujo Sangre (litros/minutos)
|
0.9
|
0.9
|
0.9
|
0.95
|
0.9
|
0.96
|
0.91
|
0.89
|
0.92
|
0.86
|
0.96
|
0.97
|
Presion Arterial Media (mm. Hg.)
|
77
|
76
|
75
|
73
|
72
|
78
|
73
|
70
|
70
|
67
|
72
|
70
|
Presion Inspiratoria Pico (cmH2O)
|
37
|
36
|
38
|
36
|
40
|
43
|
42
|
42
|
39
|
40
|
39
|
35
|
Presion Plateau (cmH2O)
|
34
|
32
|
33
|
26
|
33
|
33
|
32
|
33
|
30
|
27
|
34
|
30
|
PEEP (cmH2O)
|
20
|
20
|
20
|
20
|
20
|
20
|
20
|
20
|
20
|
20
|
22
|
18
|
Volumen Tidal (ml)
|
250
|
225
|
200
|
200
|
200
|
200
|
225
|
230
|
230
|
230
|
230
|
180
|
Frecuencia Respiratoria (Resp./min)
|
40
|
40
|
40
|
40
|
36
|
36
|
36
|
36
|
36
|
36
|
36
|
36
|
FiO2 (%)
|
100
|
100
|
100
|
90
|
90
|
80
|
80
|
80
|
80
|
80
|
75
|
75
|
PAFI
|
67
|
66
|
69
|
73
|
70
|
72
|
69
|
75
|
75
|
76
|
60
|
85
|
Ph
|
7.29
|
7.3
|
7.29
|
7.3
|
7.3
|
7.33
|
7.37
|
7.33
|
7.33
|
7.33
|
7.3
|
7.3
|
PaCO2 (mmHg)
|
50
|
47
|
47
|
46
|
45
|
41
|
37
|
41
|
40
|
40
|
40
|
46
|
PaO2 (mmHg)
|
67
|
66
|
69
|
66
|
63
|
57
|
55
|
60
|
60
|
61
|
61
|
64
|
Bicarbonato (mEq/L)
|
24
|
22
|
22
|
22
|
21
|
21
|
21
|
21
|
21
|
22
|
22
|
22
|
Saturacion Arterial de O2 (%)
|
90
|
90
|
91
|
90
|
88
|
87
|
87
|
89
|
88
|
90
|
90
|
89
|
Exceso de Base
|
-3
|
-4
|
-4
|
-4
|
-5
|
-4
|
-3
|
-4
|
-4
|
-3
|
-3
|
-4
|
Por reinicio de registros febriles al 8º día de internación se realizan nuevos cultivos y se agrega tratamiento antibiótico con colistina por sospecha de sobreinfección intrahospitalaria.
Por franca mejoría de su cuadro respiratorio con parámetros gasométricos estables y registros febriles aislados se retira sistema de remoción de CO2 extracorporea luego de 12 días de uso sin complicaciones vasculares. Con Ecografia Doppler arterial y venosa de ambas regiones femorales sin signos de trombosis. Los cultivos tomados al 8º dia de internación fueron negativos para bacterias y hongos.
Al 16º día de internación ya sin registros febriles e importante mejoría de la función ventilatoria se retira asistencia respiratoria mecánica continuando la recuperación respiratoria con ventilación no invasiva (VNI) por mascara facial completa con Radiografía de Tórax Frente que muestra infiltrados difusos bilaterales en regresión.
Marcada debilidad muscular con EMG compatible con polineuropatia del paciente critico que no altera mecánica respiratoria. (Tabla 4 Parámetros Gasométricos Día 16º)
| Hora |
6:00
|
18:00
|
| Ph |
7.42
|
7.49
|
| PaCO2 (mmHg) |
42
|
34
|
| PaO2 (mmHg) |
76
|
66
|
| Exceso de Base |
2.2
|
2.6
|
| Bicarbonato (mEq/L) |
27
|
25.5
|
| Sat.O2 (%) |
95
|
94.6
|
| PAFI |
362
|
314
|
Tabla 4. Parámetros Gasométricos Día 16º de Internacion.
La paciente pasa a sala general con O2 suplementario por bigotera nasal al día 19º de internación y es externada sin secuelas funcionales respiratorias a los 26 días de su ingreso a la institución con marcada mejoría de su cuadro respiratorio en los estudio de Diagnostico por Imágenes.(Imagen 4. Rx Torax y TAC Torax MultiSlice previas al Alta)
 |  |
 |  |

Imagen 4. Imágenes previas al alta Sanatorial (4.a Rx Torax Frente 4.b Rx Torax Perfil 4.c TAC Torax Corte Axial 4.d Corte TAC Torax Corte Sagital 4.e TAC Torax Corte Coronal
► Discusión
Si bien el término de Síndrome de Distrés Respiratorio Agudo (SDRA) es ampliamente conocido desde que fue acuñado por David Ashbaugh y colaboradores en 1967, los signos y parámetros que permiten definir el cuadro fueron revisados en múltiples ocasiones.
La ultima actualización se realizo en el año 2011, en una reunión de expertos en la ciudad de Berlín (Alemania) dando origen a lo que se conoce como Nueva Clasificación de Berlín del SDRA.8&
Según esta nueva Clasificación de Berlín el SDRA se divide en 3 niveles o grados (leve, moderado y grave o severo) de acuerdo al grado de hipoxemia que presenta el paciente con un uso mínimo de presión positiva al final de la espiración (PEEP).8&
El SDRA representa una respuesta típica del pulmón a diversas noxas que llevan a una serie variable de fases de respuesta o defensa. En forma general el daño de los capilares alveolares y de la superficie de los alveolos (Neumonocitos Tipo 1 y 2) generan una reacción que se caracteriza por infiltrados de células inflamatorias, apotosis, necrosis, formación de membranas hialinas y un aumento de la permeabilidad alveolo-capilar con el consiguiente edema alveolar.9, 12&
A pesar de que se han hecho numerosos estudios y evaluado infinidad de estrategias terapéuticas para el SDRA desde sus inicios, en la actualidad se podría concluir que casi la única estrategia terapéutica valida para su manejo es el uso de modos protectivos de asistencia mecánica respiratoria (AMR).9, 11&
Esta falta de modalidades terapéuticas esta claramente relacionada al la compleja patogénesis del síndrome que presenta múltiples señales inmuno moduladoras activadas dentro de su evolución dependiendo de la noxa que produce la lesión pulmonar.9&
Las estrategias protectivas de AMR son ampliamente conocidas desde las publicaciones de los estudios de Roy Brower y colaboradores10& y Marcelo Amato y colaboradores11& y se basan fundamentalmente en la utilización de bajos valores de Volúmen Corriente (VC, también llamados Volumen Tidal VT), en relación al peso teórico del paciente con el objeto de mantener bajas presiones (y bajos volúmenes de aire) a nivel de las vías aéreas.20&
En trabajos recientes se pudo comprobar que aun utilizando estas técnicas protectivas de AMR, la sobre distensión de alveolos en zonas de adecuada ventilación pulmonar o bien la apertura y cierre repetido de unidades alveolares colapsadas podía empeorar el daño pulmonar de los pacientes con SDRA por un mecanismo llamado “daño pulmonar inducido por el respirador” (VILI. Por las siglas en ingles de Ventilator-Induced Lung Injury).
De esta manera se acepta que aun bajo la utilización de técnicas de AMR protectivas, el solo uso de AMR puede empeorar el daño pulmonar producido por el SDRA por diferentes mecanismos definidos como barotrauma, volutrauma, atelectrauma y biotrauma.12&
En la actualidad existen varios trabajos publicados (y otros en desarrollo) en los cuales se demuestra que estrategias ultra protectivas de AMR utilizando VT 3-4 ml/kg de peso teórico asociados a dispositivos para la remoción extracorporal de CO2 que evitan la hipercapnia asociada que puede aparecer siguiendo estas estrategias ventilatorias seria la forma más eficaz de tratamiento en pacientes con SDRA severo con retención de CO2 asociada.11, 12, 13, 18, 20, 21&
El iLATM Membrane Ventilator NovalungTM es un sistema ultra compacto desechable de intercambio gaseoso extrapulmonar que funciona gracias a la presión de perfusión cardiaca del paciente. Mas allá de una fuente de oxigeno suplementario (a 10-12 Litros/min) el sistema no requiere de ninguna otra fuente de energía ni suplemento externo.7&
A través de un by pass arterio venoso femoro-femoral (Ver Figura 3) colocando dos cánulas por técnica de Seldinger (una en arteria femoral y la otra en la vena femoral contralateral) y gracias al flujo producido por el gradiente de presión arterio venosa se logra una extracción efectiva de CO2 a nivel de la membrana siempre que exista una diferencia de presión arterio venosa a nivel femoral de 60-80 mmHg. Esta membrana presenta un área de intercambio de aproximadamente 1,3 m2 y un recubrimiento especial que hace imposible las embolias gaseosas en caso de producirse una presión negativa del lado usado para el paso de la sangre. Para mantener la permeabilidad del sistema se requiere de una infusión a bajas dosis de heparina que en general no genera complicaciones hemorrágicas.7, 14, 15, 16, 17, 19, 21&
La opción de tratar a este tipo de pacientes con sistemas de oxigenación por membrana extracorpórea (ECMO por las siglas en ingles de Extra Corporeal Membrane Oxygenation) que utilizan una bomba de perfusión para generar flujo de sangre a través de un circuito de circulación extracorpórea con una membrana de oxigenación/remoción de CO2 interpuesta y permiten la oxigenación a la par de la remoción de CO2 es, en general, poco utilizada fundamentalmente por dos razones: es una técnica costosa que requiere equipamiento de alta complejidad, medios y personal altamente calificados; presenta efectos adversos y complicaciones graves de difícil resolución (respuesta inflamatoria sistémica, hemorragias severas, complicaciones quirúrgicas, etc).7, 14, 15, 16, 17, 19&
► Conclusiones
La fisiopatogenia compleja y múltiple de los casos de SDRA obliga a realizar planteos diagnósticos y terapéuticos casi específicos para cada caso en particular tanto para la estrategia de AMR a utilizar como la necesidad o no del uso de medios extracorporales de soporte respiratorio.
Aún faltan estudios randomizados y extensos que demuestren el verdadero rol de la remoción extracorpórea de CO2 en pacientes con SDRA severo e hipercapnia asociada7, 14, 15, 16, 17, 19& pero con la información disponible en la actualidad es factible concluir que en casos particulares como el descripto previamente los pacientes pueden verse altamente beneficiados por la utilización de estas técnicas y facilitar la aplicación de estrategias de AMR ultra protectiva en un intento de disminuir las posibilidades de VILI que son de alta incidencia en estos casos.
Federico Acharta
No hay comentarios:
Publicar un comentario